近日,中国农业科学院北京畜牧兽医研究所家畜营养与调控科技创新团队研究揭示了革兰氏阴性菌致病成分精准攻击宿主线粒体,引发系统性氧化损伤与炎症的共性机制。相关研究成果发表在《氧化还原生物学(Redox Biology)》上。
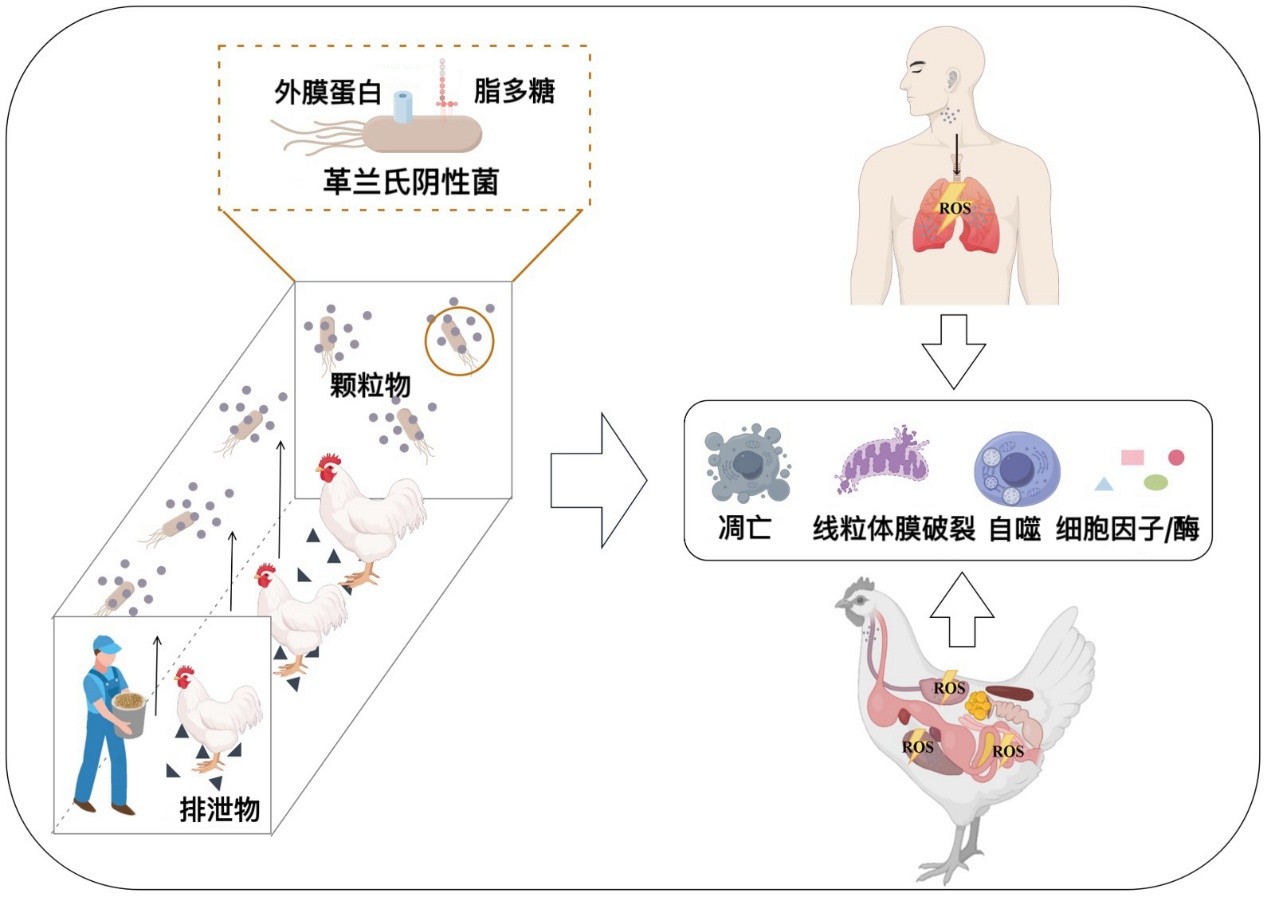
在现代家禽养殖中,鸡舍内高浓度粉尘颗粒物(PM)不仅是呼吸道刺激物,更是微生物气溶胶的载体。其中,革兰氏阴性菌释放的外膜蛋白(OMPs)和脂多糖(LPS)是两大关键毒力因子,但长期以来,它们如何协同破坏宿主细胞稳态、诱发氧化应激和炎症,缺乏统一的理论框架。
本综述创新性地提出“线粒体-活性氧(ROS)轴”作为解释机制的核心模型。研究表明,OMPs可通过破坏宿主细胞铁稳态、靶向线粒体膜通透性,诱导线粒体功能障碍和细胞凋亡,而LPS则主要通过TLR4/MyD88和TRAF6-ECSIT信号通路,触发线粒体产生大量ROS,进而激活NLRP3炎症小体,导致细胞焦亡和系统性炎症。二者虽起始路径不同,但最终汇聚于线粒体,引发ROS爆发,突破宿主的抗氧化防御系统。这一机制模型不仅为解释养殖环境中多种病原成分共同作用的病理过程提供了整合视角,也为开发针对性干预措施—如通过营养调控增强宿主抗氧化能力、改善饲养环境减少病原菌暴露—奠定了理论基础。
该论文第一作者为中国农业科学院北京畜牧兽医研究所博士研究生刘璇和郝月副研究员,通讯作者为陈亮研究员。本研究得到了国家现代农业产业技术体系和中国农业科学院科技创新工程的资助。