2019年8月8日,欧洲糖尿病学会会刊《Diabetologia》(影响因子7.113)在线发表了基因工程与种质创新团队研究论文“Adipocyte-specific disruption of the ATPase copper-transporting α in mice accelerates lipoatrophy”。 该研究揭示了脂肪组织铜过载通过增强脂肪水解和DNA损伤反应加速脂肪萎缩的重要作用。
脂肪组织是动物的主要储能和内分泌器官,不仅关乎畜禽的生产效率和肉品质,而且与人类肥胖和代谢性疾病密切相关。畜牧业生产中,饲料中添加高剂量铜能促进动物生长,提高饲料报酬。但是高铜对动物脂肪代谢的影响及其分子机理尚不明确。
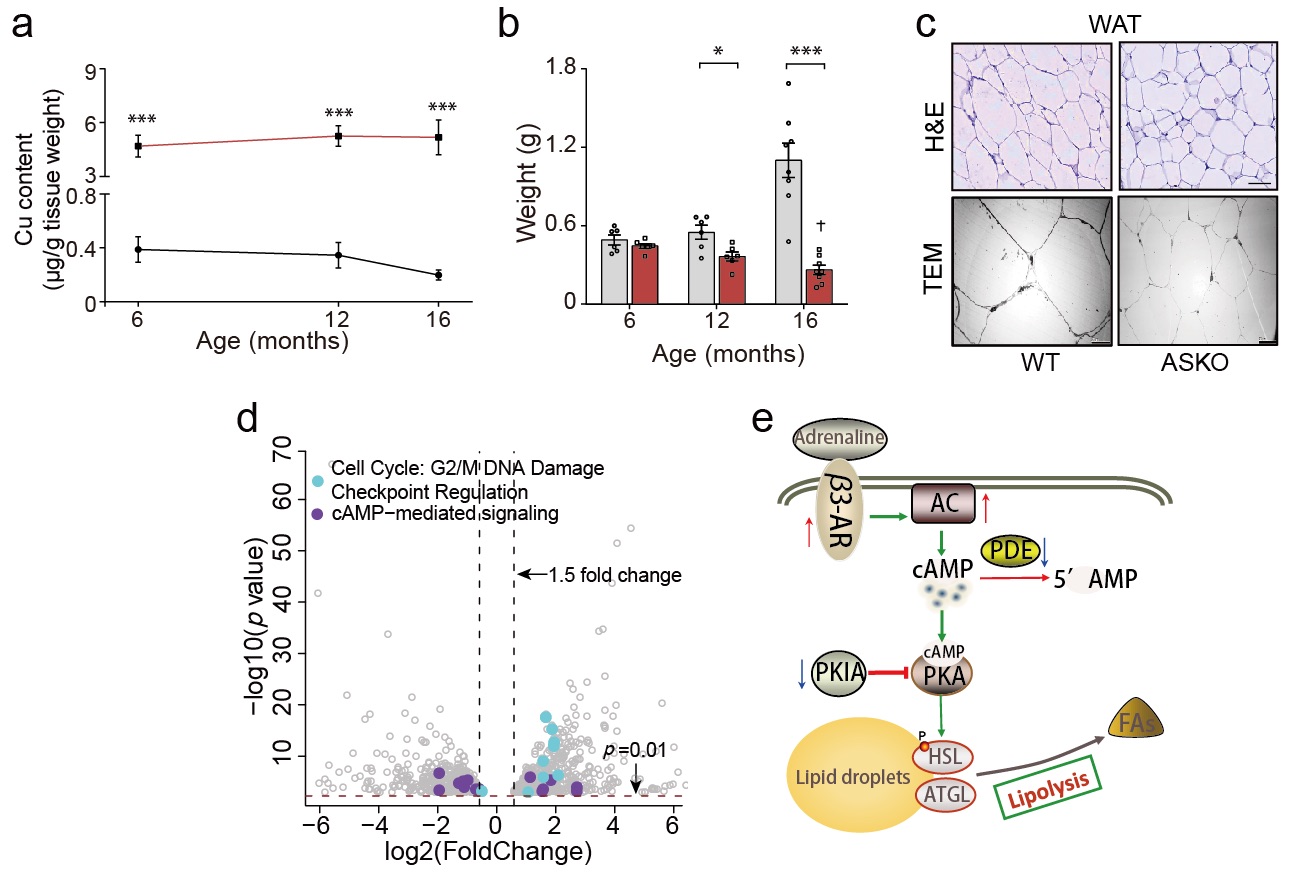
细胞铜含量受到铜转运蛋白的精细调控,ATP7A在细胞铜输出过程起着关键调控作用,可以保护细胞铜的过度积累。该研究通过构建铜离子转运蛋白ATP7A脂肪特异性敲除小鼠,该小鼠脂肪组织铜含量提高了20倍左右。这些基因修饰小鼠达到12月龄时,脂肪沉积显著减少,这种症状在16月龄时加重,并引起内分泌紊乱和糖代谢异常等代谢障碍,呈现出典型的脂肪组织萎缩。敲除小鼠在高脂饲喂条件下,7月龄时即出现上述代谢表型。该研究进一步发现脂肪铜过载增强了cAMP脂肪水解信号,加剧了DNA损伤,从而加速了脂肪细胞衰老,引起脂肪萎缩。该发现阐明了铜对动物脂肪沉积和代谢的调控作用,丰富了铜调控动物机体糖脂代谢的相关研究。
中国农业科学院北京畜牧兽医研究所为第一完成单位,基因工程与种质创新团队王彦芳研究员是本文的通讯作者,助理研究员陶聪和2017届硕士毕业生王亚君是该论文的第一作者。该研究得到了科技部973计划、国家自然科学基金、中国农科院科技创新工程和所基本科研业务费项目的资助。
论文链接:https://link.springer.com/content/pdf/10.1007%2Fs00125-019-4966-2.pdf










