中国农业科学院北京畜牧兽医研究所动物生物安全与公共卫生防控科技创新团队对程序性细胞坏死的分子调节机制及其在对抗人畜共患病原感染中的作用进行了阐述。文章在线发表在《细胞死亡与疾病(Cell Death & Disease)》上(IF=9.705)。
细胞死亡和细胞增殖的精准调控对于多细胞个体的发育和稳态以及宿主抵抗病原入侵起着至关重要的作用。细胞增殖和细胞死亡之间的平衡发生紊乱将导致机体生理机能紊乱、器官损伤,引发一系列疾病。自细胞凋亡后,近些年一系列基因调控的细胞死亡被陆续发现,包括程序性细胞坏死、细胞焦亡、铁死亡等。其中,程序性细胞坏死是病原感染中重要的炎症介导的免疫应答之一。
论文详细解析了程序性细胞坏死在流感病毒、结核分枝杆菌、沙门氏菌、致病性大肠杆菌等重要人畜共患病原感染和脓毒症中的作用机制。文章指出,不同的外界刺激,如Toll样受体、干扰素、死亡受体、病原等,均可以诱导程序性细胞坏死,蛋白激酶RIP3和其底物MLKL是程序性细胞坏死的主要执行因子。TNF与受体结合,抑制cIAP或CYLD介导的RIP1去泛素化,进而诱导细胞凋亡的产生。相反,抑制FADD 或caspase-8可以导致细胞发生程序性坏死。病原感染可激活RIP1和RIP3复合体进而诱导程序性细胞坏死。MLKL被RIP3磷酸化、寡聚化后从细胞质迁移到细胞膜致使细胞膜穿孔破裂,进而导致细胞死亡。除了RIP1-RIP3-MLKL经典程序性细胞死亡,一些包含RHIM结构域的因子,如TRIF或DAI/ZBP1,也可以介导不依赖RIP1的非经典程序性细胞坏死。该研究为深入解析程序性细胞坏死的信号通路以及利用程序性细胞坏死对抗感染性疾病提供了重要参考和思路。
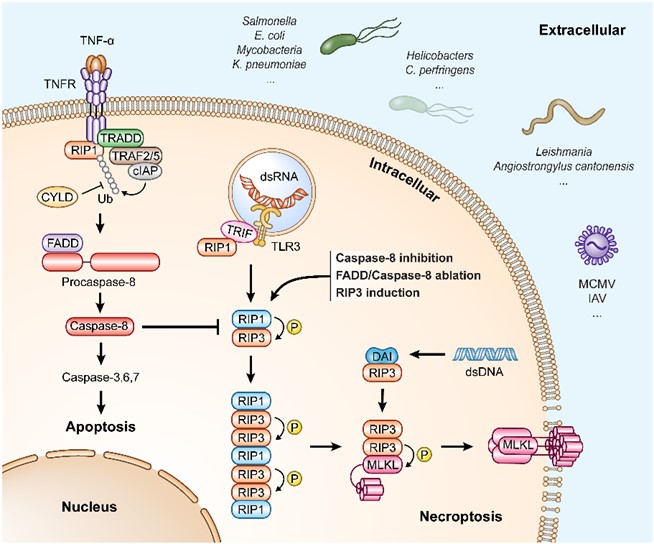
图 细胞凋亡和程序性细胞坏死的调控
张广智博士为该论文第一作者,蒋卉副研究员和丁家波研究员为共同通讯作者。该研究得到中国农业科学院科技创新工程和中国农业科学院基本科研业务费等项目的支持与资助。
原文链接:https://doi.org/10.1038/s41419-022-05066-3










