近日,中国农业科学院北京畜牧兽医研究所鸡遗传育种创新团队与合作团队研究发现了调控动物脂肪沉积和产热重要功能基因,敲除SPOP基因可以显著下调动物体重并提高动物产热能力,为动物脂肪沉积调控提供了重要理论依据。相关研究成果于发表在《公共科学图书馆:遗传学(PLOS Genetics)》上。
SPOP作为一种E3泛素连接酶,广泛参与多种生命活动调节。研究团队前期发现了该基因参与鸡先天免疫信号通路和抗病力调控,影响包括IL-1β在内的多种免疫因子水平和免疫细胞的分化。鉴于炎性因子和免疫细胞与脂肪细胞和肥胖发生的重要关联,团队继续深入探究了SPOP基因在调控脂肪沉积和能量代谢过程中的生物学功能。
研究人员以前期构建的SPOP基因敲除小鼠为动物模型,研究发现SPOP基因敲除后显著上调负责产热的线粒体内膜转运蛋白UCP1基因的表达。SPOP基因缺失后小鼠体增重明显低于对照组,蛋白组学分析表明敲除动物中上调表达的蛋白主要富集在机体产热、糖酵解/糖原异生和氧化磷酸化等信号通路上。代谢监测实验亦表明SPOP敲除动物具有较高的代谢速率和氧气消耗、对冷应激的适应能力更强。此外,在脂肪细胞中的分析表明SPOP基因的缺失会抑制脂肪的生成。
牧医所李庆贺研究员、硕士研究生刘昱宏等人为论文的共同第一作者,赵桂苹研究员、李庆贺研究员等人为论文的共同通讯作者。该研究得到科技创新2030农业生物育种重大项目等项目的资助。
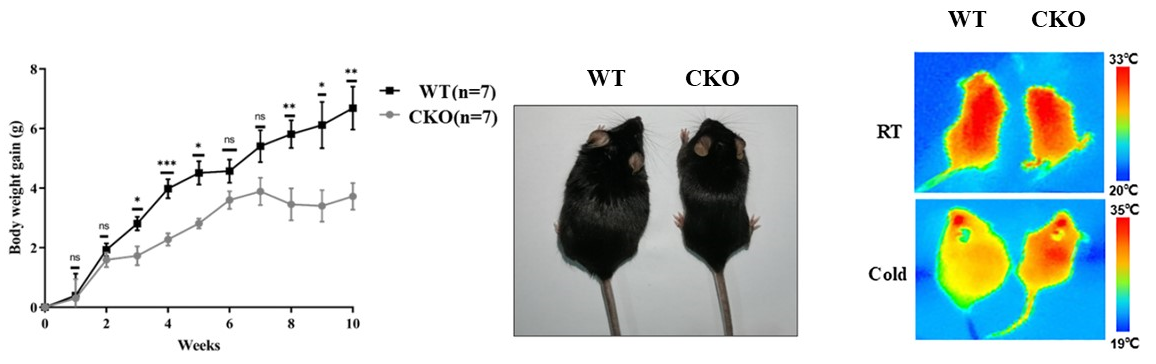
SPOP基因敲除抑制动物体重增长并促进能量代谢










